Εμβολιασμός κατά του HPV
Ο εμβολιασμός κατά του HPV είναι η πρωτογενής μέθοδος πρόληψης του καρκίνου του τραχήλου της μήτρας. Μάθετε περισσότερα διαβάζοντας τη θέση του ΠΟΥ για τον εμβολιασμό κατά του HPV.
Προσυμπτωματικός έλεγχος για τον καρκίνο του τραχήλου της μήτρας: Επιλογές εξετάσεων
HPV DNA Test: Επικυρωμένο για πρωτοβάθμιο προσυμπτωματικό έλεγχο1
Ο έλεγχος με τεστ HPV DNA ανιχνεύει τις γυναίκες που διατρέχουν κίνδυνο εμφάνισης καρκίνου του τραχήλου της μήτρας με μεγαλύτερη ευαισθησία από την κυτταρολογική εξέταση ΠΑΠ (επίχρισμα) και ο πληθυσμιακός έλεγχος με το cobas® HPV Τest όχι μόνο βρίσκει περισσότερη υψηλόβαθμη νόσο από την εξέταση ΠΑΠ, αλλά συμβάλλει και στη διατήρηση της επάρκειας του προσυμπτωματικού ελέγχου. Τα ταυτόχρονα 3 σε 1 αποτελέσματα για τον HPV 16, τον HPV 18 και τους άλλους 12 HPV τύπους υψηλού κινδύνου ξεχωριστά, επιτρέπουν τη διαστρωμάτωση του κινδύνου από τον HPV, ως βελτίωση του προσυμπτωματικού ελέγχου έναντι της υψηλότερης ειδικότητας της κυτταρολογικής εξέτασης ΠΑΠ.
Κυτταρολογική εξέταση ΠΑΠ
Από την εισαγωγή του κατά τη δεκαετία του 1940, το τεστ ΠΑΠ εκτιμάται ότι έχει συμβάλει στη μείωση κατά 70% του ποσοστού του καρκίνου του τραχήλου της μήτρας με την ανίχνευση κυτταρικών ανωμαλιών2. Ωστόσο, το τεστ ΠΑΠ, λόγω της χαμηλής ευαισθησίας του στην ανίχνευση προκαρκινικών βλαβών του τραχήλου της μήτρας3, της υψηλής μεταβλητότητας των αποτελεσμάτων μεταξύ εκπαιδευμένων επαγγελματιών από διαφορετικά εργαστήρια4 και της χαμηλής ανίχνευσης του αδενοκαρκινώματος5, έχει σημαντικούς περιορισμούς ως μια μακροπρόθεσμη, καθολική λύση για τον εντοπισμό γυναικών με κίνδυνο εμφάνισης νόσου στον τράχηλο της μήτρας.6
Co-testing (πρωτοβάθμιος προσυμπτωματικός έλεγχος με κυτταρολογική εξέταση ΠΑΠ και τεστ HPV)
Για τη βελτίωση της χαμηλής ευαισθησίας της μεμονωμένης κυτταρολογικής εξέτασης ΠΑΠ στον προσυμπτωματικό έλεγχο του καρκίνου του τραχήλου της μήτρας, ο συνδυασμός της με το HPV τεστ αποτελεί μία επιλογή. Αν και αυτή η πρακτική έχει φανεί ανώτερη για την ανίχνευση των προκαρκινικών και καρκινικών αλλοιώσεων του τραχήλου της μήτρας7, 8, είναι μόνο οριακά καλύτερη από τον μεμονωμένο προσυμπτωματικό έλεγχο με HPV τεστ και είναι αναποτελεσματική από άποψη κόστους για την υιοθέτησή της από χώρες με περιορισμένους πόρους. Όταν οι πληροφορίες των HPV γονότυπων περιλαμβάνονται στα αποτελέσματα του τεστ HPV, μπορεί να γίνει επιπλέον διαστρωμάτωση των γυναικών σε σχέση με τον κίνδυνο που παρουσιάζουν. Μία στις δέκα γυναίκες που είναι θετικές για τους HPV 16 ή/και HPV 18 έχει υψηλόβαθμη νόσο που δεν έχει ανιχνευτεί από την μεμονωμένη κυτταρολογική εξέταση.9
Επιλογές διαλογής για τα μη φυσιολογικά αποτελέσματα του προσυμπτωματικού ελέγχου
Βιοδείκτες ή κυτταρολογική εξέταση ΠΑΠ
Οι αλγόριθμοι πρωτοβάθμιου προσυμπτωματικού ελέγχου με HPV τεστ συχνά περιλαμβάνουν την κυτταρολογική εξέταση ΠΑΠ ως κατάλληλη μέθοδο διαλογής. Ωστόσο, οι νέες εξετάσεις που βασίζονται στην τεχνολογία της διπλής χρώσης βιοδεικτών προσφέρουν σημαντικά πλεονεκτήματα σε σχέση με την παραδοσιακή προσέγγιση. Αντί για την αναζήτηση αλλαγών στη μορφολογία των κυττάρων, οι οποίες ενδέχεται να μην παρατηρηθούν λόγω υποκειμενικότητας, τα αποτελέσματα που βασίζονται στην ταυτόχρονη έκφραση του p16 και του Ki-67 στο ίδιο κύτταρο υποδεικνύουν ξεκάθαρα και με περισσότερη αντικειμενικότητα ότι η λοίμωξη από HPV παρουσιάζει σημεία ογκογόνου μετασχηματισμού.
Η κυτταρολογική εξέταση CINtec® PLUS έχει έγκριση FDA και σήμανση CE-IVD και είναι μία εξέταση διπλής χρώσης των βιοδεικτών p16 και Ki-67 με αντικειμενικό αποτέλεσμα. Μπορεί να χρησιμοποιηθεί για τη διαλογή των θετικών αποτελεσμάτων στον πρωτοβάθμιο προσυμπτωματικό έλεγχο με HPV τεστ, στη διαχείριση περιστατικών με ασυμφωνία στο co-testing (θετικό HPV τεστ/φυσιολογικό ΠΑΠ) και στη διαχείριση των κυτταρολογικών ευρημάτων ASC-US (άτυπα πλακώδη κύτταρα απροσδιόριστης σημασίας) και LSIL (χαμηλού βαθμού ενδοεπιθηλιακή αλλοίωση πλακώδους επιθηλίου). Εάν εντοπιστεί συνύπαρξη των p16 και Ki-67 στο ίδιο κύτταρο, αυτό υποδεικνύει ότι η HPV λοίμωξη έχει ξεκινήσει τον μετασχηματισμό των κυττάρων. Αυτή η πληροφορία βοηθά τους κλινικούς ιατρούς να προτείνουν με βεβαιότητα περαιτέρω έλεγχο μόνο στις ασθενείς που θα επωφεληθούν περισσότερο από αυτόν.
Η κυτταρολογική εξέταση CINtec® PLUS είναι η πρώτη εγκεκριμένη εξέταση διαλογής με βιοδείκτες που χρησιμοποιεί την τεχνολογία της διπλής χρώσης για την ταυτόχρονη ανίχνευση των p16 και Ki-67, ώστε να παρέχεται ισχυρή ένδειξη της παρουσίας HPV λοίμωξης που έχει ξεκινήσει τον μετασχηματισμό των κυττάρων.
Μάθετε περισσότερα.
Γονοτύπηση HPV
Κάποιες χώρες χρησιμοποιούν τη γονοτύπηση του HPV για τη διαλογή των αποτελεσμάτων της κυτταρολογικής εξέτασης ΠΑΠ ή του co-testing. Οι πληροφορίες από τη γονοτύπηση του HPV διαστρωματώνουν περαιτέρω τον κίνδυνο που διατρέχει μία ασθενής, διευκολύνοντας τη λήψη αποφάσεων για τη φροντίδα της.
Οι γονότυποι 16 και 18 του HPV σχετίζονται σχεδόν με το 70% όλων των περιπτώσεων του καρκίνου του τραχήλου της μήτρας10. Η εστίαση σε αυτούς τους γονότυπους παρέχει στους κλινικούς ιατρούς χρήσιμα στοιχεία διευκολύνοντας τη λήψη θεραπευτικών αποφάσεων. Ο γονότυπος HPV 16 ενέχει μεγαλύτερο κίνδυνο εμφάνισης προκαρκινικών βλαβών και καρκίνου του τραχήλου της μήτρας σε σχέση με τους άλλους γονότυπους, ενώ ο γονότυπος HPV 18 βρέθηκε στο 57% των περιστατικών με αδενοκαρκίνωμα του τραχήλου της μήτρας11. Τα άτυπα αδενικά κύτταρα, ο πρόδρομος του αδενοκαρκινώματος του τραχήλου της μήτρας, ανιχνεύονται πιο δύσκολα με την κυτταρολογική εξέταση ΠΑΠ.12
Επιλογές διαλογής στον προσυμπτωματικό έλεγχο
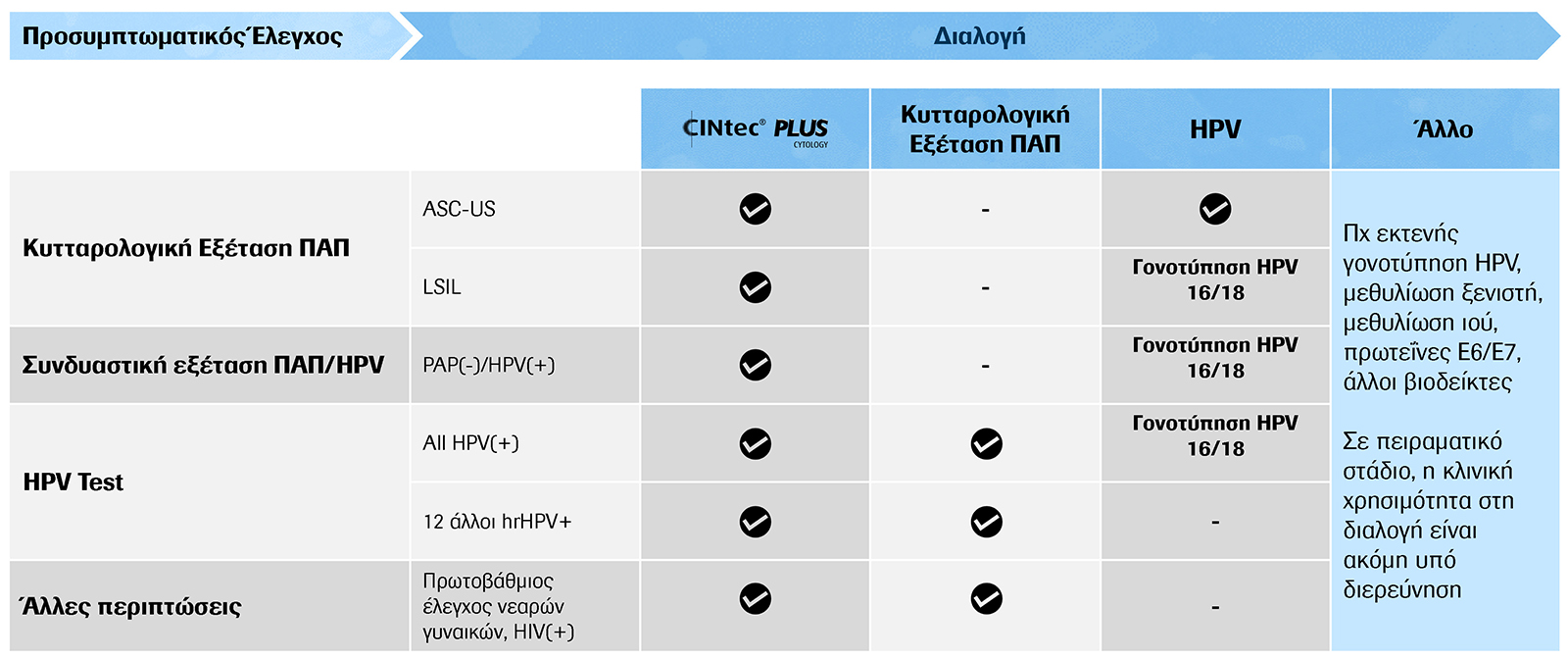
Στρατηγικές διάγνωσης για τον καρκίνο του τραχήλου της μήτρας: Οι επιλογές σας
Χρώση αιματοξυλίνης και ηωσίνης (H&E) μόνο
Η αξιολόγηση των βιοψιών του τραχήλου της μήτρας με τη χρήση της H&E χρώσης μόνο (αξιολόγηση της μορφολογίας), ενδέχεται να οδηγήσει σε ψευδώς αρνητικά και σε ψευδώς θετικά αποτελέσματα, με επακόλουθο να χαθεί νόσος ή να γίνει υπερθεραπεία.
Χρώση H&E + ανοσοϊστοχημική (IHC) χρώση p16: Συνιστώμενη στρατηγική13
Η αξιολόγηση της ανοσοϊστοχημικής χρώσης του p16 επικουρικά μαζί με τη χρώση H&E αυξάνει τη διαγνωστική συμφωνία μεταξύ των παθολογοανατόμων. Η ιστολογική εξέταση CINtec® είναι η μόνη εξέταση του p16 βιοδείκτη που έχει εγκριθεί από τον FDA για κλινική χρήση και για In Vitro Διαγνωστική χρήση για την αξιολόγηση των δειγμάτων βιοψίας τραχήλου του μήτρας. Όταν χρησιμοποιείται η ιστολογική εξέταση CINtec® από τους ειδικούς, ανιχνεύονται 23.8% περισσότερα περιστατικά με υψηλόβαθμη νόσο σε σύγκριση με τη χρώση H&E μόνο14.
Μάθετε περισσότερα.
Κολποσκόπηση
Η κολποσκόπηση πραγματοποιείται όταν τα αποτελέσματα των εξετάσεων του προσυμπτωματικού ελέγχου για την πρόληψη του καρκίνου της μήτρας δείχνουν μη φυσιολογικές αλλαγές στα κύτταρα του τραχήλου ή εάν μια γυναίκα είναι θετική σε έναν από τους γονότυπους υψηλού κινδύνου του HPV, όπως ο γονότυπος 16 ή 18. Οι επιστημονικές κατευθυντήριες οδηγίες των εταιρειών ASCCP, ASCP και ACS συνιστούν άμεση εξέταση με κολποσκόπηση για τις γυναίκες με φυσιολογική κυτταρολογία που είναι θετικές για HPV 16 ή HPV 18.
Μερικές φορές κατά τη διάρκεια της κολποσκόπησης πραγματοποιείται και βιοψία, ώστε να συλλεχθούν δείγματα ιστού από περιοχές που φαίνονται ύποπτες. Οι διαγνωστικές πληροφορίες που λαμβάνονται από τα δείγματα βιοψίας τραχήλου της μήτρας βοηθούν στην καθοδήγηση για τη φροντίδα της ασθενούς ή στη λήψη θεραπευτικών αποφάσεων. Τα δείγματα αυτά αποστέλλονται για εργαστηριακή ανάλυση στον παθολογοανατόμο, ώστε να ανιχνευτούν προκαρκινικές αλλοιώσεις αν υπάρχουν.
